- 关键字: 代表性成果之四:生物大分子结构模拟与精确测定 发布者:宣传部 发布时间:2009-02-24 22:02:24 点击数: 8847次
|
代表性研究成果四
|
基础类或
应用基础类或基础性类
|
成果为第一完成单位
|
本室固定
人员参加
名单
|
是否
保密
|
|
生物大分子结构模拟与精确测定
|
基础类
|
是
|
黎占亭
周佳海
曹春阳
吴厚铭
夏宗芗
|
否
|
生物分子如多肽、蛋白质和DNA的三维高级结构是其产生催化、代谢、离子通道、信号传导及遗传功能的基础,是重要前沿研究领域之一。模拟生物大分子的高级结构,不但有助于深入理解大分子形成高级结构的机理及关键作用力,还有可能产生新的小分子结构,选择性地识别生物分子,从而达到调控其生物功能、发展药物先导化合物的目的, 而直接的精确确定生物大分子三维结构, 可以使人们在分子或原子水平上了解生物大分子发挥生物活性的作用机制,更利于阐述其功能; 生物分子三维结构信息,特别是生物大分子与其小分子配体的复合物的结构信息,也为小分子调节剂的设计提供了重要的依据,为了解小分子配体的作用机制提供了最直观的方法,有助于重大疾病的预防和治疗、新型高效药物和疫苗的研发等。
在过去五年里,我们通过分子设计、X-射线晶体学和核磁共振等方法在此领域开展了一系列研究,并在以下几个方面取得重要进展: 1) 利用分子内氢键作为驱动力,诱导芳酰胺类分子形成各种折叠、螺旋、类b-折叠的模拟二级结构; 2)利用核磁共振(NMR)技术开展生物大分子溶液结构及靶蛋白与药物分子相互识别机制研究;3)利用X-衍射晶体学技术研究蛋白质三维结构-功能关系。共发表57篇论文,其中影响影子大于5的有10篇,被他人引用225次,其中部分成果作为第二单位获得2006年教育部自然科学二等奖。其中,受到较大关注的论文包括:
|
Acc. Chem. Res. 2008, 41, 1343
|
Peptidomimetics专辑特邀论文
|
|
Angew. Chem. Int. Ed. 2005, 44, 5725
|
被评为VIP论文,纠正了国际理论化学界长期接受的有机分子中F不能形成分子内氢键的观点
|
|
Chem. Asian J. 2006, 1, 766
|
被评为该期刊创刊以来引用最高的论文:
http://www3.interscience.wiley.com/journal/112140232/home/2451_mostcited.html
|
|
J. Org. Chem. 2007, 72, 870
|
被列为2007 年度J. Org. Chem. 引用最多的20篇论文之一。
|
|
J. Org. Chem. 2008, 73,1745
|
被Synfacts 撰文评介(2008, 5, 475)
|
以下是所取得的代表性重要进展具体内容如下:
1.1 折叠、螺旋和扩展型的生物模拟二级结构
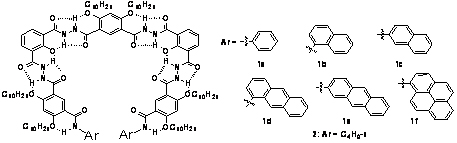
利用F×××H-N氢键组装螺旋结构:长期以来,国际学术界认为中性有机氟化合物中的氟元素不能作为有效的氢受体形成氢键。Pauling在其《Nature of the Chemical Bond》一书中就提出:“It is interesting that in general F atoms attached to C do not have significant power to act as proton acceptors in the formation of hydrogen bonds in the way that would be anticipated from the large difference in electronegativity of fluorine and carbon”。瑞士理论化学家Dunitz于2004年曾撰文专门评述这一观点(ChemBioChem 2004, 5, 614)。我们推测,在适当设计的氟代芳酰胺分子中,应有可能形成稳定的五元环和六元环F×××H-N氢键。为此,我们合成了一系列线性分子,通过晶体结构分析、核磁及红外等手段证明了有机氟化合物分子内F×××H-N氢键的存在。在此基础上,我们又首次成功利用分子内F×××H-N氢键诱导这类芳酰胺寡聚物形成一类全新的分子折叠体和螺旋体结构。下面结构代表了一个五聚体和七聚体产生的螺旋体结构。该类螺旋体的内径约在0.6 nm,在氯仿中它们能通过分子间F×××H-N氢键有效结合各种有机铵离子(A×HCl和B×HCl)。由于化合物B有一个手性中心,诱导CD光谱研究表明,受强烈的分子间氢键的驱动,其单分子手性可以通过络合转移到络合物中,诱导该类寡聚体产生螺旋偏差。本项工作2005年在Angew. Chem. Int. Ed.(2005, 44, 5725)上发表,并被评为VIP论文。
.jpg)
分子内氢键诱导芳酰胺折叠结构:我们还基于同样原理,分别设计了两类线性芳酰胺衍生物,通过改变形成分子内O×××H-N氢键的基团的位置,组装出两类折叠体结构1和2。核磁和荧光实验证明这两类分子能比较有效的识别有机铵离子和糖类衍生物。并且,手性铵离子和糖分子可以通过结合作用把手性传递到整个络合物,产生超分子手性。
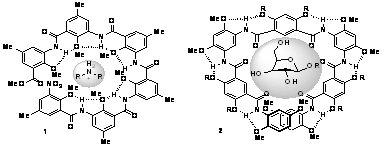
1.2 基于折叠或螺旋结构的分子识别
利用氢键调控产生结合适配性分子受体:在氢键介质的芳酰胺三聚体两端引入两个卟啉片断,由于两个板块的刚性结构特征,该类分子内两个卟啉片断处于平行排列堆积的状态。在缺电性的客体比如萘四甲酰亚胺等存在下,分子间的供体-受体相互作用取得客体分子插入到两个卟啉之间,从而使主体分子内的氢键强度降低。这种折叠性分子受体在结合客体的前后表现出弹性的构象变化,显示出这种结合具有明显的结构适配性特征。
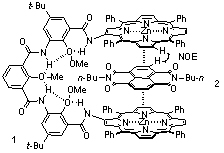
基于折叠结构的非对映选择性结合:在前期工作中,我们曾发展出一类氢键驱动的芳酰胺折叠体,它们可以在氯仿等弱极性溶剂中高效结合糖类分子(J. Am. Chem. Soc. 2004, 126, 12386)。在此基础上,我们对骨架进行修饰,在其两端引入手性的脯氨酸片段。该手性片段诱导折叠骨架产生手性偏差。CD实验表明,R,R-和S,S-构型的折叠体与葡萄糖对映体可以形成对映体结构的络合物,而同一手性的折叠体与对映体葡萄糖形成非对映体络合物。前者的CD光谱信号强度相同,但方向相反,而后者形成不对称的CD信号。利用定量的荧光滴定实验可以测定出相应络合物的结合常数,下面两个非对映体的络合物的结合常数可以形成高达144倍的差别,显示出手性折叠体络合的高度选择性。
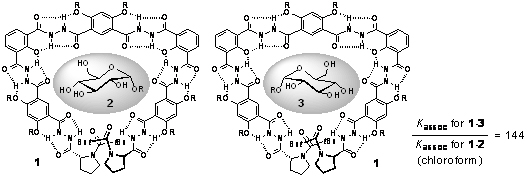
1.3 叠结构的双股复合物结构
生物结构模拟的一个重要方面是模拟DNA等生物大分子的复合结构。我们在前期工作中已经确立,分子内氢键可以诱导芳酰胺寡聚体形成刚性的扩展平面型二级结构(J. Org. Chem. 2004, 69, 6221)。进一步对该结构板块进行修饰,在分子的一侧同时引入能够自结合的酰胺和尿等,通过其协同多氢键作用诱导平面二聚体结构的产生。1H NMR研究表明,尽管单一的酰胺或尿基驱动形成二聚体的稳定性很小,但随着分子带的延长和酰胺或尿基结合单元数量的增加,在氯仿中该类分子能够通过分子间的氢键驱动形成稳定的双股二聚体结构。本项工作也说明了分子内氢键诱导芳酰胺分子带产生刚性结构对分子间氢键形成的有效性。
.jpg)
1.4 三维高级结构的模拟构筑
利用模拟折叠结构产生单分子层膜、构筑囊泡:囊泡等是研究生物膜及细胞构筑的重要结构。我们在前期工作中已经确立,分子内氢键可以诱导芳酰肼寡聚体形成折叠的构象(J. Am. Chem. Soc. 2004, 126, 12386)。进一步的在侧链中引入酰胺并延长链的长度,我们又合成了化合物1-3。在极性溶剂如甲醇中,芳环间堆积作用诱导其产生柱状结构,进一步发生柱状结构的堆积,从而形成直径分布较为单一的囊泡。这是利用模拟二级结构产生三维囊泡结构的第一个例子。
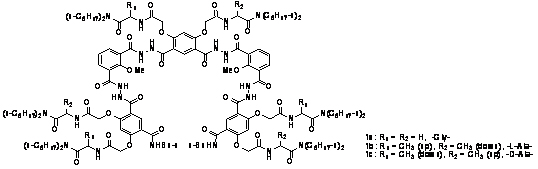
模拟折叠结构在凝胶相分离状态下的动态手性传递:在前期工作中,我们发现芳酰胺折叠体在弱极性溶剂中高效地结合糖类分子(J. Am. Chem. Soc. 2004, 126, 12386)。在此基础上,我们又设计了折叠结构1,在其外侧引入长的脂肪链,在两端引入大的芳环片段。这类分子能够固定多种类型的有机溶剂,形成凝胶。加入糖类分子,其能够通过对糖的络合形成增强的堆积作用,从而提高了凝胶化溶剂的作用。并且,CD光谱研究表明,这种络合作用可以把糖的手性传递到整个堆积结构中,产生明显的超分子手性放大效应。这种超分子手性的放大也具有所谓的“Sergeant and soldiers”效应,其动态堆积过程具有明显的时间依赖性。通过详细的CD光谱研究,我们提出了其堆积-成核-延长-凝胶化的组装机理过程。这一过程类似于生物矿化及软骨形成过程中生物及无机小分子的簇集。
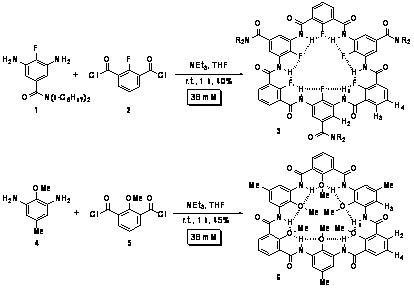
1.5 模拟二级结构促进有机反应¾大环结构的构筑和醚的水解加速
通过分子内氢键诱导构筑大环体系:生物酶通过预组装构象产生协同的结合域,从而达到催化反应的目的。我们发现,这一原理同样适用于模拟的折叠分子体系。利用分子内氢键指导分子片段和中间体的构象或形状,我们可以利用间-苯二胺与间-苯二甲酰氯,一步形成6个酰胺键,形成相应的环酰胺分子。这类分子由于具有较高的刚性和平面性,在弱极性溶剂中可以与富勒烯和蒄等发生分子间堆积,形成1:1的络合物。当利用2,6-吡啶二甲酰氯为前体时,我们可以得到2 + 2的环酰胺产物。这样就可以通过改变单体的结构得到不同尺度的环番结构,为进一步探索该类环番的识别和组装性能提供了基础。
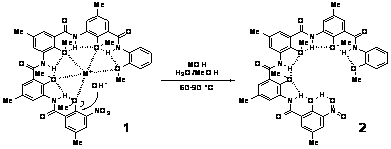
折叠结构促进的苯甲醚水解:生物酶可以通过对金属离子的络合催化很多水解反应。我们发现,在水相中,并入硝基的芳酰胺折叠体能够通过其甲氧基氧络合碱金属碱MOH(M = Li, Na, K)的金属离子,从而促进硝基取代的苯甲醚的水解。我们详细研究了这一促进作用的动力学过程。结果表明,相对于参照化合物,水解速率可以提高4-6倍。这一结果说明氢键驱动的分子折叠可以发生在强极性溶剂中,这与上述在甲醇等极性溶剂中开展的囊泡组装研究是一致的。
2.1 利用核磁共振技术进行生物大分子溶液结构及与小分子配体相互作用研究
短链蝎毒素BmTx3B、BmKK2、BmKK4和BmP08结构与功能研究:BmTx3B主要采用其b-折叠表面与钾通道相互作用(b-型结合模式)。它与Kv通道结合时由于缺少关键位置的盐桥和疏水作用,具有低的选择性和亲合力。相反它与Kca1.1通道的结合由于显示较强的芳香残基p-p相互作用,导致较高选择性和亲合力,同时其在结合过程表现出了慢结合、慢解离的动力学现象。
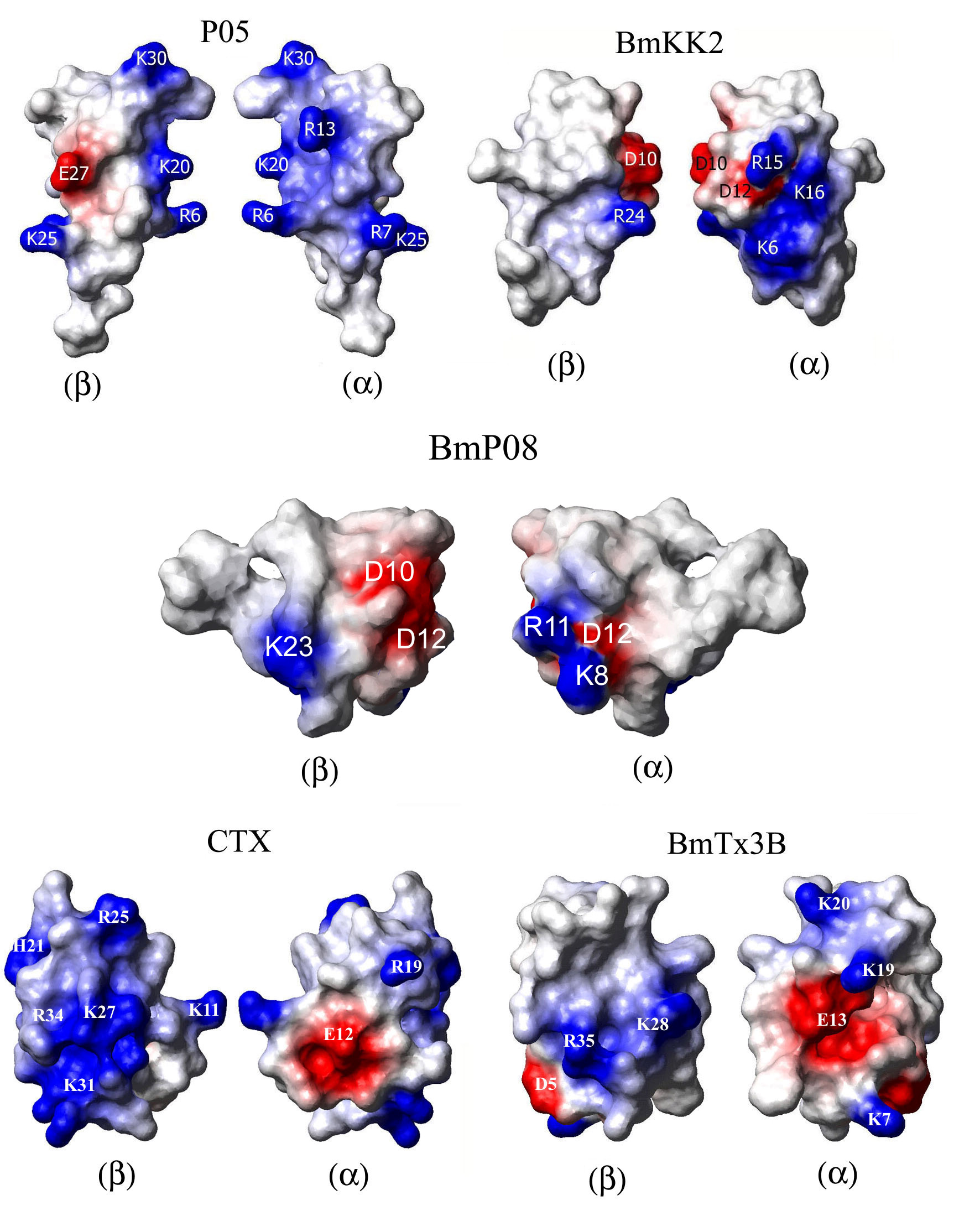
BmKK2/Kca2.2通道复合物模型发现BmKK2与具有狭窄“前庭”的Kca2.2通道间有良好的静电和疏水作用,其作用表面主要发生在a-螺旋面(被定义为a-结合模式)。BmKK4的结构特征是其第四个半胱氨酸前的两个关键性残基为Asp和Arg,导致其b-折叠中生成一个“b-突起”和盐桥。“b-突起”和盐桥的存在改变了其b-折叠的走向,也不利于其与Kv通道的结合。分子对接与动力学模拟研究发现BmKK4与Kca2.2通道间形成了多个氢键和盐桥,其作用表面主要发生在毒素的a-螺旋和b-折叠二级结构的侧面(被定义为a/b-型结合模式)。
BmP08由31个氨基酸残基组成,它的一级序列与其它的短链蝎毒素相比有显著差别,序列中保守Cys残基间的氨基酸数目配置也发生了变化,同源序列比较认为它可能属于一类全新的蝎毒素家族。结构研究表明BmP08具有短链蝎毒素特征性的CS-a/b motif整体折叠方式,但又表现出与其它短链蝎毒素不同的结构特征,b-折叠结构很短,仅由两条含两个氨基酸残基的b-链组成,螺旋结构是310-螺旋而不是在短链蝎毒素中常见的a-螺旋。此外,BmP08的三维结构局部构象,表面电荷分布和表面功能区残基的分析,表明它的靶离子通道和结合模式可能不同于已知的各类蝎毒素。
长链蝎毒素BmP09、BmK-bIT和BmKaIT01三维结构与功能研究:BmP09含有66个氨基酸残基,电生理实验表明它能够特异性的作用于小鼠肾上腺嗜铬细胞(MACC)中的Kca1.1钾离子通道(IC50 值为27 nM),而对钠离子和钙离子通道都没有作用。BmP09是目前为止发现的唯一一个对大电导,Ca2+激活的钾离子通道有高效的选择性抑制活性的长链蝎毒素,具有长链a型蝎毒素的典型结构特征,一条a-螺旋、三股反平行b-折叠、以及几个loop和转角共同构成了它的核心结构。通过同源建模和分子模拟的方法分析BmP09/Kca1.1钾通道复合物模型发现,在BmP09中围绕在核心残基Lys41周围的Tyr34、Tyr36、Phe39和Tyr57等芳香残基是决定蝎毒素选择性结合Kca1.1钾离子通道的主要因素,这些芳香残基与钾通道相应位点的芳香型残基间的p-p相互作用是蝎毒素结合Kca1.1通道的一个普遍的重要特征。
BmK-bIT一级序列比较表明该毒素具有兴奋性昆虫毒素典型的结构特征:一对移位的二硫键,与b-型兴奋性蝎毒素高度同源,电生理实验表明该毒素可以产生兴奋性毒素特有的药理特征,因此该毒素属于b-型兴奋性蝎毒素。溶液结构研究表明除却Bj-xtrIT中存在一个额外的a0-螺旋外,该毒素与b-型兴奋性昆虫蝎毒素Bj-xtrIT和BmK IT-AP具有相似的整体折叠方式。此外,电生理研究还发现该毒素对哺育动物的钠通道也具有一定的抑制作用,通过与具有抗哺育动物活性的b-型蝎毒素Ts1和CssIV进行比较,认为可能是位于连接b2与b3的loop区域中的疏水性残基和Glu15在这一生理功能中发挥着重要作用。
.jpg)

BmKaIT01具有很强的抗昆虫活性及较弱的抗哺育动物活性,一级序列比较发现该毒素与抗昆虫a-型长链毒素具有很高的同源性(> 70 %),因此该毒素可作为抗昆虫a-型长链蝎毒素一天然突变子。溶液结构研究表明,BmKaIT01具有a-型蝎毒素典型的CS-a/b motif结构特征。结构比较发现,BmKaIT01的三维结构与抗昆虫a-型蝎毒素LqhaIT、LqqIII的溶液结构及a-like型蝎毒素BmK M1的晶体结构相类似,而与抗哺育动物经典a-型蝎毒素AaH II差别较大,主要体现在连接分子中二级结构单元的loop及C-末端区域;研究还发现BmKaIT01分子在溶液中存在异构现象,这可能是由于Asn9 ~ Tyr10之间的顺式肽键在溶液中发生顺反异构进而引起毒素分子整体构象的变化,从而使得该毒素表现出抗昆虫活性的同时兼有较弱的抗哺育动物活性。

基质金属蛋白酶12(MMP-12)与γ-KBA抑制剂的识别机制研究:巨噬细胞金属弹性蛋白酶(MMP-12)是基质金属蛋白酶家族的重要成员之一。相比较其他的MMP成员,其独特之处在于它主要是在巨噬细胞内表达的,所表达的酶原大约54kDa,但很容易自动切除前肽和C末端类血红素区域而形成的催化区域,其水解弹性蛋白的比活在基质金属蛋白酶家族中最高。巨噬细胞金属弹性蛋白酶和巨噬细胞与人类的疾病密切相关,这些疾病包括高致死率的动脉血管粥样硬化、慢性阻塞性肺疾病和肺气肿。因此MMP-12是体内很重要的的一个药物靶点,寻找其配体分子具有很重要的现实意义。通过对MMP12与小分子配体γ-KBA类抑制剂复合物的溶液三维结构的研究,可以加深了对MMP-12的结构与功能关系的认识,也有助于合理设计MMP-12高选择性、高亲和性的抑制剂。
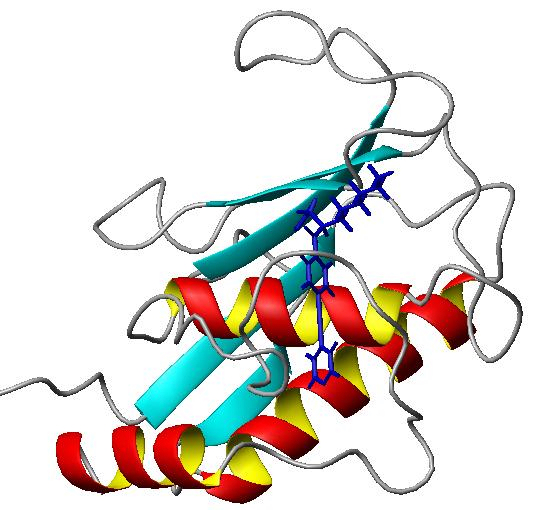
通过距离约束和扭转角约束进行分子动力学与模拟退火运算,并结合计算机分子模拟与显示技术,得到了一组最优构象来代表MMP-12与小分子配体复合物的溶液三维结构。在此溶液结构中,位于α-螺旋hB上的残基Leu214、Thr215、His218、选择性loop上的Pro238-Thr239-Tyr240的主链原子及残基Tyr240的侧链共同构筑了S1’活性位点的口袋口。选择性loop上的疏水性残基Val235、Phe237、Thr239、Lys241、Val243的侧链则构筑了S1’活性位点的口袋外壁。小分子抑制剂的P1’基团比较完满地充盈了S1’活性口袋,与其口袋外侧的疏水残基形成了较强的疏水亲脂相互作用。S1’活性口袋的大小、及组成活性口袋残基的性质决定了配体分子与MMP-12作用选择性和特异性的结构因素。
3.1 利用X-衍射技术测定生物分子三维结构及分子间相互作用
谷胱甘肽转移酶GSTk:谷胱甘肽转移酶是在生物体内广泛存在的一类酶,它对异源物质(包括药物、致癌物和外来化学物质及其代谢物)具有解毒作用,并能防止自由基的活性产物对细胞膜上的脂质造成损害。谷胱甘肽转移酶有多种亚型,其中k型(GSTk)是从线粒体基质中分离得到的一个新亚型。我们生长得到两种晶型的单晶,首先利用同晶置换法解析得到晶型B中不对称单元一个分子的结构,然后以该分子作为搜索模型分子,用分子置换法对晶型A进行结构解析,最终确定其相位并完成结构修正。晶体结构分析揭示底物类似物谷胱甘肽亚磺酸分子结合在活性部位,亚磺酸基团中的一个氧原子与16位的丝氨酸中的羟基形成氢键。结构比较结果还发现,尽管GSTk与GSTq的序列同源性只有19%,但三维结构却非常相似,因此在GST超家族蛋白中k型可能与q型更接近一些。本项工作2005年发表于Protein Science杂志。
.jpg)
来源于植物的新型核糖核酸酶马干铃蛋白的结构与功能关系研究:马干铃蛋白是一种从植物马干铃的根部提取出来的新型蛋白,早期研究认为它具有RNA N-糖苷水解酶活性。我们利用天然提取的蛋白制备了单晶,通过多对同晶置换的方法解决了相位问题并最终完成了2.2Å分辨率的结构精修,首次结合X-射线晶体结构测定和质谱法确定了该蛋白的一级序列。三维结构搜索和比较发现,马干铃蛋白可能是一种新型的S-类型核糖核酸酶,这一推论得到了生化测活实验的验证。进一步的研究发现,马干铃蛋白晶体不具有RNA N-糖苷水解酶活性,天然来源蛋白的活性是由夹杂其中的少量b-型马干铃蛋白所造成的。本项工作的成果2004年发表于Cell 杂志子刊Structure上。
.jpg)
.jpg)
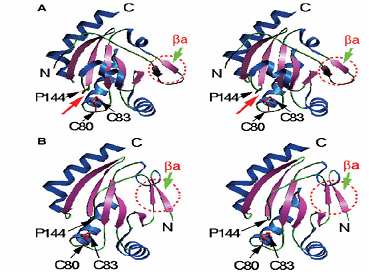
二硫键氧化还原酶CcmG的结构-活性关系研究:CcmG又名DsbE,在细胞色素c的成熟过程中有非常专一性的还原活性。我们完成了大肠杆菌CcmG蛋白及两个突变体的高分辨率晶体结构测定和精修,在结构分析的基础上,首次发现CcmG的N-端的b-折叠是维持正确折叠和活性中心结构所必须的; 并首次阐明了CcmG 的指纹区的具体功能:Pro144和Glu145是指纹区的关键氨基酸残基,Pro144为顺式构型,通过范德华作用和C-H×××O氢键而稳定活性中心二硫键,Glu145通过形成盐桥和氢键网络而进一步稳定活性中心结构;指纹区的Tyr141在CcmG与DsbD蛋白结合时发生构象变化。本项工作的成果2006年发表于Proteins: Struct. Funct. Bioinform.上。
 沪ICP备05005485号
沪ICP备05005485号